Das Lungenkarzinom ist eine maligne Veränderung des Lungengewebes und die häufigste Ursache für krebsbedingte Todesfälle. Die meisten Fälle sind mit dem langjährigen Rauchen verbunden. Die Krankheit wird im Allgemeinen histologisch entweder als kleinzelliges Lungenkarzinom (SCC) oder Nicht-kleinzelliges Lungenkarzinom klassifiziert (NSCLC). Das molekulare Profiling des Tumors ermöglicht eine weitere Unterscheidung des biologischen Verhaltens des Tumors, der Prognose und der Behandlungsmöglichkeiten. Häufig auftretende Symptome sind Husten, Dyspnoe Dyspnoe Dyspnoe (Atemnot/Luftnot), Gewichtsverlust und thorakale Beschwerden. Die regionale und metastasierende Ausbreitung verursacht je nach Lokalisation und betroffenem Organ zusätzliche Symptome und Komplikationen. Verwandte paraneoplastische Syndrome Paraneoplastische Syndrome Paraneoplastische Syndrome umfassen Hyperkalzämie Hyperkalzämie Hyperkalzämie, Hyponatriämie Hyponatriämie Hyponatriämie, Lambert-Eaton-Syndrom, Cushing-Syndrom Cushing-Syndrom Cushing-Syndrom, Polydermatomyositis und Dermatomyositis Dermatomyositis Dermatomyositis (DM). Die endgültige Diagnose und das Staging werden durch eine Biopsie, Nachweis genetischer Mutation mit Biomarker-Tests und die Bildgebung gestellt. Die Therapie richtet sich nach dem Karzinomstadium und dem damit verbundenen molekularen Profil. Das Lungenkarzinom hat eine insgesamt schlechte Prognose.
Kostenloser
Download
Lernleitfaden
Medizin ➜
Untertypen:

Adenokarzinom der Lunge:
Ein schlecht differenziertes (solides) Adenokarzinom mit vielen Zellen mit Muzinvakuolen
Untertypen:

Plattenepithelkarzinom bei Lungenbiopsie:
Histopathologie eines schlecht differenzierten SCC der Lunge (H&E-Färbung)

Kleinzelliges Lungenkarzinom:
Die Tumorzellen (siehe Pfeile) weisen Merkmale eines kleinzelligen Karzinoms auf, zu denen Kernformung, ein hohes Kern:Zytoplasma-Verhältnis und feine oder Salz-und-Pfeffer-Chromatin-gemusterte Kerne bei der H&E-Färbung gehören.
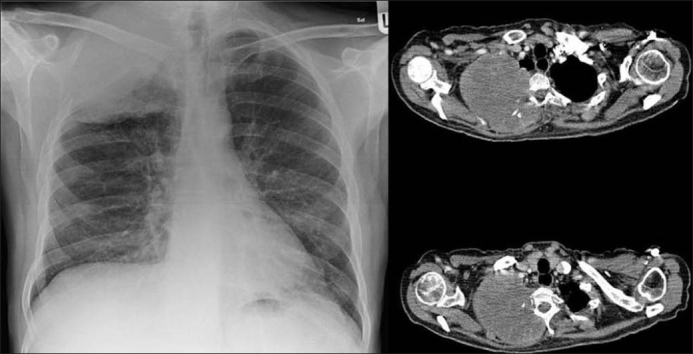
Pancoast-Tumor:
Das Röntgenthorax auf der linken Seite zeigt eine Neoplasie der rechten Lunge, die in die Rippe und die Brustwand eindringt. Die Computertomographie auf der rechten Seite zeigt den Tumor, der in die Rippen, die Brustwand und die Brustwirbel eindringt.
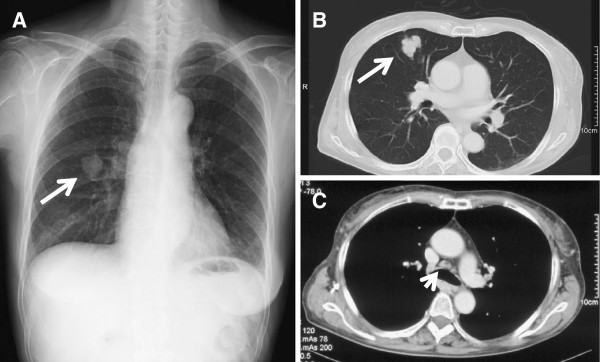
Röntgen-Thorax und CT-Scan bei Diagnose:
(A): Röntgenaufnahme der Brust, die einen Schatten einer Raumforderung in der rechten mittleren Zone zeigt (Pfeil).
(B, C): Konventionelles Thorax-CT mit einer 30-mm-solitären Raumforderung in S5 der rechten Lunge (Pfeil) und mediastinaler Lymphadenopathie (Pfeilspitze).
Anwendung weiterer Bildgebung, um das Ausmaß der Erkrankung für Staging-Zwecke zu bestimmen:

Bronchoskopie
Lungenkarzinom (Pfeile) im linken Bronchus, wie mit einem Bronchoskop gesehen
Folgende Tests sind mögliche Befunde für Lungenkarzinom:
TNM-Stadien für SCLC und NSCLC nach IASLC 2017
| Stadien | Beschreibung |
|---|---|
| Tx | Der Primärtumor kann nicht beurteilt werden. |
| T0 | Kein Hinweis auf einen Primärtumor |
| Tis | Karzinom in situ |
| T1 | Tumor ≤ 3 cm, umgeben von
Lunge
Lunge
Lunge: Anatomie oder viszeraler
Pleura
Pleura
Pleura, ohne Invasion des Hauptbronchus:
|
| T2 | Tumor > 3 cm aber ≤ 5 cm oder:
|
| T3 | Tumor > 5 cm aber ≤ 7 cm oder assoziierte Tumorknötchen im gleichen Lappen wie der primäre Tumor oder direkte Invasion der Brustwand Brustwand Brustwand, des N. phrenicus oder des Perikards parietalis |
| T4 | Tumor > 7 cm oder assoziierte Tumorknötchen in einem anderen ipsilateralen Lappen als dem primären Tumor oder Invasion in das Zwerchfell Zwerchfell Zwerchfell (Diaphragma), Mediastinum Mediastinum Mediastinum und große Gefäße, Herz, große Gefäße, Luftröhre Luftröhre Trachea, Speiseröhre Speiseröhre Ösophagus (Speiseröhre), N. laryngeus recurrens, Wirbelkörper oder Karina |
| Stadien | Beschreibung |
|---|---|
| Nx | Kann regionale Lymphknoten Lymphknoten Lymphsystem nicht beurteilen |
| N0 | Keine regionalen Lymphknotenmetastasen |
| N1 | Ipsilaterale peribronchiale und/oder hiläre Lymphknoten Lymphknoten Lymphsystem und intrapulmonale Lymphknotenbefall |
| N2 | ipsilaterale mediastinale und/oder subkarinale Lymphknotenbeteiligung |
| N3 | Kontralaterales Mediastinum Mediastinum Mediastinum und große Gefäße, kontralaterales Hilus, ipsilaterales oder kontralaterales Skalenus oder supraklavikulärer Lymphknotenbefall |
| Stadien | Beschreibung |
|---|---|
| M0 | Keine Fernmetastasen |
| M1 | Fernmetastasen:
|
| Phasengruppierung | TNM-Stufe |
|---|---|
| Okkulte |
|
| 0 |
|
| I |
|
| II |
|
| III |
|
| IV |
|
| Stufe (SCLC) | Beschreibung |
|---|---|
| Very Limited Disease |
|
| Limited Disease |
|
| Extensive Disease |
|
Operation:
Chemotherapie:
Strahlentherapie:
Targeted Therapien:
Immuntherapie:
| Stadium (NSCLC) | Behandlungsansatz |
|---|---|
| Stufe I–II |
|
| Stufe III |
|
| Stufe IV* |
|
| Stufe (SCLC) | Beschreibung |
|---|---|
| Limited disease |
|
| Extensive disease* |
|
Die Modifikation von Risikofaktoren ist wirksamer als das Screening, um den Tod durch Lungenkarzinom zu reduzieren. Ein Screening wird vor allem in den USA durchgeführt. In Deutschland werden keine flächendeckenden Vorsorgeuntersuchungen/Screenings empfohlen.